前言
膜電解是電滲析和電解相結(jié)合的技術(shù),根據(jù)膜組合方式的不同,可分為單陽膜法、單陰膜法和雙極膜法等,其中單陽膜法操作簡單,應(yīng)用較為普遍。
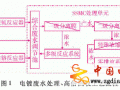
本實(shí)驗(yàn)利用陽離子交換膜自制膜電解裝置(如圖1所示),研究不同陰極膜室電解質(zhì)溶液對(duì)廢水中CLi2+的去除率和回收方式的影響。
1 實(shí)驗(yàn)
1.1 實(shí)驗(yàn)裝置
自制膜電解裝置,如圖1所示。離子交換膜采用科氏公司生產(chǎn)的陽離子交換膜,膜片有效尺寸為60 mm×80 mm,數(shù)量為2片。槽體有效容積為2 500 mL,膜盒容積為900 mLo陽極:釕銥錫鈦涂層,100 mm×100 mm;銥鉭鈦涂層,100 mm×1 00 mm o陰極:銅片,80 mm×80 mmo

1.2 分析方法
采用二乙氨基二硫代甲酸鈉萃取光度法對(duì)廢水中的Cu2+進(jìn)行分析。
1.3 實(shí)驗(yàn)方法
將2 500 mL含銅電鍍廢水裝入廢水槽內(nèi),在陰極膜室中加入電解質(zhì)溶液,異極間距為6 cm,施加電壓為6 V o以一定的、時(shí)間間隔采集水樣,并記錄實(shí)驗(yàn)現(xiàn)象。廢水性質(zhì)和實(shí)驗(yàn)條件,如表1所示。

2 結(jié)果與討論
2.1 不同電解質(zhì)溶液下廢水中Cu2+的去除率依據(jù)表1所列條件,分別采用硫酸銅、氫氧化鈉、草酸和氨水為陰極膜室電解質(zhì)溶液進(jìn)行含銅電鍍廢水的膜電解實(shí)驗(yàn),在各電解質(zhì)溶液條件下,廢水中Cu2+的去除率與電解時(shí)間的關(guān)系,如圖2所示。

由圖2可知:隨著電解過程的進(jìn)行,廢水中Cu2+的去除率呈升高趨勢(shì)。四種不同的電解質(zhì)對(duì)Cu2+的去除率在一定條件下由高到低的順序?yàn)椋喊彼⒉菟帷溲趸c、硫酸銅。以氨水為電解質(zhì)時(shí),電解5h,廢水中Cu2+的去除率為94. 71%;以硫酸銅為電解質(zhì)時(shí),電解6 h,廢水中C1-i2+的去除率為39. 29 %0以草酸為電解質(zhì)的膜電解過程,從電解第4h到電解第6h的實(shí)驗(yàn)中,廢水中Cu2+的去除率的曲線斜率為35. 58;以氨水為電解質(zhì)的膜電解過程,從電解第2h到電解第4h的實(shí)驗(yàn)中,廢水中CL12+的去除率的曲線斜率為34. 33 0以氨水為電解質(zhì)時(shí),電解4h,廢水中Cu2+的去除率達(dá)到90. 72%,廢水中Cu2+的質(zhì)量濃度為10. 16 mg/Lo和采用其他電解質(zhì)相比,采用氨水作為電解質(zhì)處理含銅電鍍廢水具有反應(yīng)時(shí)間短、去除效率高、設(shè)備容積小、廢水處理成本低以及投資省等特點(diǎn)。
在以氨水作為電解質(zhì)的膜電解過程中,廢水中出現(xiàn)一定量的絮體,對(duì)廢水中的絮體進(jìn)行過濾,并定量酸溶檢測(cè),其中C1一i2+的質(zhì)量濃度約占膜電解過程中去除的Cu2+的40%0因此,在以氨水為電解質(zhì)的實(shí)驗(yàn)過程中,Cu2+的去除包括Cu2+在電場(chǎng)力作用下通過陽離子交換膜的遷移、Cu2+在濃度差的作用下通過離子交換膜的滲析以及在廢水中形成含CLi2+的絮體三種途徑。在用其他三種電解質(zhì)進(jìn)行膜電解實(shí)驗(yàn)時(shí),沒有觀察到廢水中存在絮體,因此,采用其他三種電解質(zhì)的膜電解過程中,Cu2+的去除以電場(chǎng)力作用和濃度差作用為推動(dòng)力來完成。
2.2 不同電解質(zhì)溶液下廢水中Cu2+的質(zhì)量濃度
在各電解質(zhì)溶液條件下,廢水中Cu2+的質(zhì)量濃度與電解時(shí)間的關(guān)系,如圖3所示。

由圖3可知:隨著電解過程的進(jìn)行,廢水中CLi2+的質(zhì)量濃度呈下降趨勢(shì)。在采用草酸和氨水作為電解質(zhì)時(shí),Cu2+的質(zhì)量濃度的下降幅度較大。以氨水為電解質(zhì)時(shí),電解5h,廢水中Cu2+的質(zhì)量濃度由109. 43 mg7L降至5.79 mg/L;以草酸為電解質(zhì)時(shí),電解6h,廢水中Cu2+的質(zhì)量濃度由109. 43mg/L降至20. 92 mg7L;以硫酸銅為電解質(zhì)時(shí),電解6h,廢水中CLi2+的質(zhì)量濃度由35. 75 mg/L降至23.10 mg7Lo
在以草酸為電解質(zhì)的膜電解過程中,廢水中的C1_i2+在pH值為4~5時(shí)沒有得到充分的釋放,隨著電解過程的進(jìn)行,廢水條件發(fā)生變化,Cu2+逐漸被釋放,在電解2h時(shí),廢水中Cu2+的質(zhì)量濃度達(dá)到最大值。
2.3 Cu2+的回收方式
在膜電解過程中,廢水中CL12+的回收按照不同電解質(zhì)溶液表現(xiàn)出不同的方式。
(1)硫酸銅
在以硫酸銅為陰極膜室電解質(zhì)的實(shí)驗(yàn)過程中,由于陰極上不斷析出H2,因此,陰極電解質(zhì)溶液的pH值逐漸升高。在此溶液條件下,通過離子交換膜的Cu2+,一部分與溶液中的OH一結(jié)合,形成CLI(OH)2沉淀物,另一部分在陰極上析出銅。
(2)氫氧化鈉
在以氫氧化鈉為陰極膜室電解質(zhì)的實(shí)驗(yàn)過程中,溶液處于強(qiáng)堿性條件下,通過離子交換膜的Cu2+,一部分與溶液中的OH一結(jié)合,形成Cu(OH)2沉淀物,另一部分在陰極上析出銅。
(3)草酸
在以草酸為陰極膜室電解質(zhì)的實(shí)驗(yàn)過程中,H2不斷在陰極上析出,溶液中OH一的濃度逐漸增加。溶液中存在草酸根和OH一,通過離子交換膜的Cu2+,一部分與溶液中的草酸根和OH一結(jié)合,形成草酸銅配位物和Cu(OH)2沉淀物,另一部分在陰極上析出銅。
(4)氨水
在以氨水為陰極膜室電解質(zhì)的實(shí)驗(yàn)過程中,在電場(chǎng)力和滲析作用下通過離子交換膜進(jìn)入陰極膜室的Cu2+,一部分與氨水結(jié)合,形成銅氨配位物,另一部分在陰極上析出銅。此外,在廢水中形成的絮體,作為Cu2+的沉淀物,成為廢水中Cu2+的去除和回收的另一種形式。
3 結(jié)論
(1)和采用其他電解質(zhì)相比,采用氨水作為電解質(zhì)處理含銅電鍍廢水具有反應(yīng)時(shí)間短、去除效率高等特點(diǎn)。
(2)以氨水為電解質(zhì)的膜電解過程,廢水中Cu2+的去除率最高oCu2+的去除途徑包括Cu2+通過離子交換膜進(jìn)入陰極膜室和在廢水槽中形成絮體,使得Cu2+從廢水中得以去除。以草酸、氫氧化鈉、硫酸銅為電解質(zhì)的膜電解過程,廢水中Cu2+的去除主要是Cu2+通過離子交換膜進(jìn)入陰極膜室而得以去除。