1.2.4 檸檬酸處理的桔子皮吸附劑。
1.2.4.1 0.1mol/L檸檬酸濃度下經(jīng)不同溫度處理的桔子皮吸附劑。往5g異丙醇(20%)-NaOH處理的桔子皮吸附劑(SOP)中,加入0.1mol/L的檸檬酸溶液100m,l分別在25、50、80℃下攪拌2h,抽濾,在室溫下水洗多次至pH值為7,抽濾后,并在55℃干燥箱中烘干24h,即得異丙醇(20%)-NaOH-0.6mol/L檸檬酸經(jīng)不同溫度處理的桔子皮吸附劑,代號分別為0.1SCA2、0.1SCA5、0.1SCA8。
1.2.4.2 0.6mol/L檸檬酸濃度下經(jīng)不同溫度處理的桔子皮吸附劑。往5g異丙醇(20%)-NaOH處理的桔子皮吸附劑(SOP)中,加入0.6mol/L的檸檬酸溶液100m,l分別在25、50、80、120℃下攪拌2h,抽濾,在室溫下水洗多次至pH值為7,抽濾后在55℃干燥箱中烘干24h,即得異丙醇(20%)-NaOH-0.6mol/L檸檬酸經(jīng)不同溫度處理的桔子皮吸附劑,代號分別為0.6SCA2、0.6SCA5、0.6SCA8、0.6SCA12。1.2.4.3 不同濃度檸檬酸在80℃下處理的桔子皮吸附劑。往5g異丙醇(20%)-NaOH處理的桔子皮吸附劑(SOP)中,分別加入0.3、0.6、0.9mol/L的檸檬酸溶液100m,l在80℃下攪拌2h,抽濾,在室溫下水洗多次至pH值為7,抽濾,并在55℃干燥箱中烘干24h,即得異丙醇(20%)-NaOH-不同濃度檸檬酸(80℃)處理的桔子皮吸附劑,代號分別為0·3SCA8、0·6SCA8、0.9SCA8。
1.2.4.4 異丙醇(20%)-0.1mol/LCA(25℃)處理的桔子皮吸附劑。往5g異丙醇(20%)處理的桔子皮吸附劑(AOP)中,加入0.1mol/L的檸檬酸溶液100m,l在室溫下攪拌2h,抽濾,在室溫下水洗多次至pH值為7,再抽濾,并在55℃干燥箱中烘干24h,即得異丙醇(20%)-0.1mol/L檸檬酸(25℃)處理的桔子皮吸附劑,代號為0.1CA。
1.2.4.5 異丙醇(20%)-0.6mol/LCA(25℃)處理的桔子皮吸附劑。往5g異丙醇(20%)處理的桔子皮吸附劑(AOP)中,加入0.6mol/L的檸檬酸溶液100m,l在室溫下攪拌2h,抽濾,在室溫下水洗多次至pH值為7,抽濾,并在55℃干燥箱中烘干24h,即得異丙醇(20%)-0.6mol/L檸檬酸(25℃)處理的桔子皮吸附劑,代號為0.6CA。
1.2.5 金屬離子Cu2+的滴定方法。用移液管分別抽取5ml樣品放入250ml錐形瓶中,準確加入25ml標準EDTA(0·001mol/L),加1~2滴0.1%二甲酚橙指示劑,溶液呈黃色,再加入少量的30%的六次甲基四胺,將溶液調(diào)成亮黃色。用硝酸鉛標準溶液滴定至紫紅色,即為終點。記錄消耗的硝酸鉛的體積Vf,計算出銅吸附平衡時濃度Cf。
其計算公式:
式中,q為生物吸附劑吸附金屬離子的容量(mol/kg);Ci為Cu2+初始濃度(mol/L);Cf為吸附平衡時濃度(mol/L);V為溶液體積(L);W為吸附劑干重(kg)。
2 結果與分析
2.1 溶液的酸度對生物吸附劑桔子皮吸附銅離子的影響 在酸性范圍內(nèi)選擇了pH值為1·5、2·2、3·6、4·8、5·4、6·2、6·57個梯度。先稱取0.1g的代號為OP的吸附劑放入100ml小燒杯中,并加入0.001mol/L的不同酸度的Cu2+溶液50m,l放在電動攪拌器下攪拌10h,取出過濾至100ml燒杯,再用5ml移液管移取5ml濾液至250ml錐形瓶中,根據(jù)滴定方法滴定,記錄消耗的硝酸鉛的體積Vf,從而計算出吸附平衡時Cu2+的濃度以及初始濃度。并以pH值為橫坐標,生物吸附劑吸附金屬離子的容量為縱坐標,繪制生物吸附劑桔子皮在不同酸度下對重金屬銅的吸附圖。將剩余10種改性的生物吸附劑桔子皮進行同樣的試驗,并繪圖。由圖1可知,pH值對不同吸附劑吸附銅離子量有很明顯的影響。在強酸環(huán)境下,桔子皮吸附劑對銅離子的吸附量都很小,在一定范圍內(nèi),隨著pH值的增大,吸附量也隨之增加;pH值繼續(xù)增加,吸附量又逐漸減小。值得注意的是,隨著吸附的進行,體系的pH值是降低的,這是因為重金屬(Cu2+)與吸附劑表面上的—COOH和—OH等官能團上的H+發(fā)生了離子交換,交換下來的H+進入溶液中,導致溶液體系的pH值降低。
該試驗條件下,桔子皮吸附劑對銅離子吸附的最佳pH值范圍為4.5~5.5,選擇pH值5.2為適合于吸附Cu2+的最佳值。工業(yè)廢水一般呈弱酸性,因而在這種情況下最有利于生物材料對金屬離子的吸附。未經(jīng)處理的OP的吸附量最小,經(jīng)過氫氧化鈉處理后吸附量有所提高,未經(jīng)氫氧化鈉處理的0.1CA、0.6CA的吸附量在高酸度下增加幅度大些,但最大吸附量與氫氧化鈉處理的接近;但是再經(jīng)過檸檬酸處理后的吸附劑吸附量有了大幅度的增加。
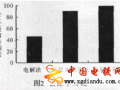
接著用同種方法研究了在同一溫度下用不同濃度檸檬酸修飾的吸附劑0.1SCA8、0·3SCA8、0.6SCA8、0.9SCA8對Cu2+的吸附量隨pH值變化的情況。由圖2可知,在pH值為5.5條件下,吸附劑對銅離子的吸附量達到了最大,而且?guī)追N吸附劑對銅離子的吸附量非常接近。說明吸附量并不隨著檸檬酸的濃度的升高而增大,其原因可能是當檸檬酸濃度過大時,會產(chǎn)生空間位阻,從而抑制了金屬離子的吸附。
考察不同溫度下檸檬酸修飾的吸附劑0·6SCA2、0·6SCA5、0.6SCA8、0.6SCA12對Cu2+的吸附量隨pH值變化的情況。由圖3可知,最佳pH值下,不同吸附劑吸附銅離子的吸附量大小順序是:0.6SCA8>0.6SCA12>0.6SCA5>0·6SCA2。在常溫下修飾的吸附劑的吸附量明顯小于其他3個吸附劑,同時也可以看出,并不是溫度越高吸附量就越大。其原因是,升高溫度可以形成檸檬酸酐濃縮體,它可以與纖維素上的羥基結合形成酯連接,從而增加與正電性金屬離子鍵合的活性點;當溫度進一步增加時,會導致膠聯(lián)度增大,從而抑制了金屬離子的吸附。
2.2 吸附時間對生物吸附劑桔子皮吸附銅離子的影響 在25℃下,分別稱取0.1g桔子皮吸附劑放入11個帶塞錐形瓶
中,并分別加入0.001mol/L的被吸附的Cu2+溶液(調(diào)好pH值為5.2)100m,l放在電動攪拌器下攪拌,定時10、20、30、50、60、90、120、240、480、900、1440min,取出過濾至100ml燒杯,根據(jù)滴定方法滴定,記錄消耗的硝酸鉛的體積Vf,計算出Cu2+吸附平衡時濃度和初始濃度。