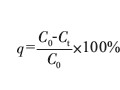(華南理工大學 環(huán)境科學與工程學院,廣東 廣州 510006)
摘要:探討了預處理一氧化沉淀一曝氣生物濾池(BAF)組合工藝處理混合電鍍廢水的可行性。結果表明:采用該組合工藝處理混合電鍍廢水具有一定的可行性;當水力停留時間為3h時,BAF對CODcr,,CN-和Cu2+的去除率分別可達50%,83%和80%。
關鍵詞: 混合電鍍廢水;預處理;氧化沉淀;曝氣生物濾池
中圖分類號:X 703 文獻標識碼:A 文章編號:1000-4742(2012)06-0038-04
O前言
目前,電鍍廢水的處理技術大多是基于對廢水完全分流的前提下,針對不同種類的污染物選用不同的處理工藝進行處理。然而,對于早期的電鍍工業(yè)園區(qū),由于受當時規(guī)劃的影響,廢水管道往往錯綜復雜,同時廢水處理廠的占地及構筑物均已受限,加之其生產工藝落后,“跑、冒、滴、漏”現(xiàn)象普遍存在,因此,對廢水進行完全分流處理難度較大。此外,由于廢水中有機物成分復雜且可生化性差,因此,出水中的CODcr.往往難以達到排放標準。對此,本文探討了預處理一氧化沉淀一曝氣生物濾池( BAF)組合工藝處理混合電鍍廢水的可行性。
1 實驗
1.1 實驗材料
實驗所用廢水取自廣東肇慶某電鍍工業(yè)園區(qū)的
廢水調節(jié)池,其水質指標為:CODcr 300~500mg/L,Cr(VI) 30~80 mg/L,CN- 50~120 mg/L,Ni2+ 60~150 mg/L,Cu2+ 30~50 mg/L, pH值2~3。
實驗所用藥品:NaClO(有效氯的質量分數(shù)為10%),Ca(OH)2 ,FeS04•7H2O,Na2S,H2S04,聚丙烯酰胺(PAM),以上試劑均為分析純。
1.2實驗方法與裝置
1. 2.1預處理
取原水500 mL,調節(jié)pH值后加入質量分數(shù)為10%的FeS04溶液,攪拌反應一段時間后,加入質量分數(shù)為0.3%的PAM,沉淀后取上清液測定CN-,Cr( VI),Ni2+,Cu2+的去除率。
1.2.2氧化沉淀
取500 mL經預處理后的上清液,調節(jié)pH值后加入NaCl0溶液,攪拌反應一段時間后,加入適量的FeS04•7H2O,Na2S和質量分數(shù)為10%的H2S04,最后加入質量分數(shù)為0.3%的PAM,沉淀后取上清液測定CN-,Ni2+,Cu2+的去除率。
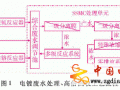
1.2.3 BAF反應器
材質為有機玻璃柱,內徑為85 mm,有效高度為0.8 m。生物填料選用粒徑為2~5 mm的球形輕質陶粒。采用上流式連續(xù)進水方式,氣水比為
5:1。
1.3分析方法
廢水的pH值,CODcr,,CN-,Cr( VI),Ni2+,Cu2+的檢測均參照國家環(huán)境保護總局制定的標準檢測分析方法。
2結果與討論
2.1 最佳預處理條件的確定
混合電鍍廢水中含有多種污染物,尤其是同時含有Cr( VI)和CN-,可采用先兩級破氰再還原沉淀Cr(VI)的方法處理此類廢水[1-2]。但對于CN-的質量濃度較高,且含有氰化亞銅、檸檬酸、EDTA的配合物等的廢水,若直接進行破氰勢必會消耗大量的氧化劑,造成處理成本過高。研究表明:FeS04不僅可以在廣泛的pH值范圍內還原Cr( VI)[3],還可以與CN-反應生成鐵氰化物[4-5]。
2.1.1初始pH值的影響
取500 mL原水,調節(jié)pH值,按理論量[ρFeS04•7H2OρCr( VI)]的1. 67倍加入FeS04•7H2O,攪拌反應15 min后加入PAM,沉淀后取上清液檢測各項指標,考察初始pH值對預處理效果的影響,實驗結果,如圖1所示。

由圖1可知:初始pH值在6~10范圍內,Cr( VI)的去除率均達到99%以上;初始pH值為6時,CN-的去除率最高,但此時Cu2+和Ni2+的去除效果不好;初始pH值為10時,各項污染物均有較好的去除效果,且CN-的去除率達到52%。文獻[4-5]指出:當pH值在6~10范圍以外時,F(xiàn)e2+對CN-的去除率基本不變。綜合上述分析,初始pH值取10為宜。
2.1.2 FeS04•7H2O的影響
取500 mL原水,在初始pH值10,反應時間15min的條件下,考察FeS04•7H2O的質量濃度對預處理效果的影響,實驗結果,如圖2所示。

由圖2可知:隨著FeS04•7H2O的質量濃度的增加,CN-的去除率逐漸升高;當FeS04•7H2O的質量濃度大于1 200 mg/L時,CN-的去除率穩(wěn)定在50%左右。加入適量的FeS04•7H2O有助于去除Ni2+,因為在堿性條件下,F(xiàn)e2+可水解生成Fe(OH)2和Fe(OH)3,并可形成具有絮凝、吸附作用的多核羥基配位物,與重金屬離子發(fā)生共沉淀[6-7]。此外,Cr(OH)3在pH值為9時也具有良好的絮凝作用,從而可與鐵系氫氧化物及重金屬離子發(fā)生共沉淀作用。然而,當FeS04•7H2O的質量濃度過高時,反而會降低Cu2+和Ni2+的去除率。因為Fe2+的質量濃度過高時,會導致溶液的pH值急劇下降,從而使Cu(OH)2和Ni(OH)2的絮體減少,同時破壞了共沉淀體系。綜合上述分析,確定FeS04•7H2O的質量濃度為1 200 mg/L。
2.1.3 反應時間的影響
在初始pH值10,F(xiàn)eS04•7H2O 1 200 mg/L的條件下,考察反應時間對預處理效果的影響,實驗結果,如圖3所示。
由圖3可知:在堿性條件下,當反應時間為5 min時,Cr(VI)的去除率達到99%以上;當反應時間為15 min時,各項污染物的去除率均趨于平緩。綜合上述分析,反應時間取15 min為宜。
通過上述分析,確定最佳預處理條件為:初始pH值10,F(xiàn)eS04•7H2O 1 200 mg/L,反應時間15min。此時,Cr( VI),CN-,Cu2+,Ni2+的去除率分別可達99%,52%,90%,83%,出水中Cr( VI)的質量濃度小于0.5 mg/L。

2.2氧化沉淀處理
廢水經預處理后,各類污染物均得到了有效的去除,尤其是將需要還原的Cr(VI)沉淀去除,為后續(xù)的完全氧化破氰創(chuàng)造了有利的條件,可避免氧化劑和還原劑的反復加入。
預處理后,廢水中殘余的氰化物以及重金屬離子大部分以配位物的形式存在。此時對廢水進行氧化沉淀處理,一方面是為了完全破除氰化物,使廢水達到排放標準;另一方面是為了破除金屬配位物的配位鍵,使金屬離子游離出來,最后通過沉淀去除。
2.2.1氰化物的去除
以NaCl0溶液為氧化劑去除氰化物的堿性氯化法已相當成熟,筆者通過實驗得出最佳工藝條件為:初始pH值10,mNaClO:mCN一=13.33,反應時間40 min,出水中CN-的質量濃度小于0.3 mg/L。
NaCl0溶液破氰分為不完全氧化和完全氧化兩個階段[8]。筆者通過實驗認為:NaCl0溶液破氰的兩個階段并沒有絕對的界限,可以在同一反應內及不調節(jié)pH值的條件下進行。由于破氰過程中有金屬離子游離出來消耗了堿度,使溶液的pH值下降,促進了完全氧化階段的進行。
2.2.2重金屬的去除
NaCl0溶液破氰后,大部分被配位的重金屬離子得以游離出來生成金屬氫氧化物沉淀,但仍有1~2 mg/L的Cu2+和7~8 mg/L的Ni2+難以去除。對于超標的Cu2+,可適當加入Na2S去除,但由于NiS的溶度積較低,加入Na2S仍不能使Ni2+達標排放。筆者通過分析電鍍生產工藝及金屬配位物的穩(wěn)定常數(shù)后認為,超標的Ni2+很可能以EDTA配位物的形式存在。為此,破氰后可加入適量的FeS04•7H2O,然后再加入Na2S,可使Cu2+,Ni2+均達到排放標準。
2.3 BAF生物處理
廢水經氧化沉淀處理后,出水中的CN-及重金屬離子均達到排放標準,但CODcr仍在200 mg/L左右,需對其進一步處理。BAF集生物氧化及吸附截留于一體,對低懸浮物和低CODcr,廢水具有很好的處理效果[9],同時對廢水中的Cu2+也具有較好的去除效果[10]。此外,有學者[11]通過研究認為:微生物可從CN-中獲得碳、氮等養(yǎng)料,從而對廢水中的CN-有一定的去除效果。
筆者對BAF反應器進行污泥接種后,先加入面粉掛膜,再用經預處理后的廢水進行一個月的培養(yǎng)馴化,最后分別用于處理預處理后的出水及氧化沉淀處理后的出水,考察BAF的水力停留時間(空床停留時間)對廢水中CODcr,,CN-的去除效果,實驗結果,分別如圖4和圖5所示。


由圖4可知:CODcr和CN-的去除率均隨著水力停留時間的延長而升高,最高分別可達45%和
58%,并在4h后趨于穩(wěn)定。由此說明BAF可以承受一定質量濃度的CN-和重金屬離子的沖擊,并對CODcr,和CN-保持一定的去除效果。
由圖5可知:當BAF處理氧化沉淀處理后的出水時,其對CODcr,和CN-的去除率均顯著提高,在水力停留時間為3h時,去除率分別可達50%和83%。分析其原因可能有以下兩點:一是雖然CN-可以為微生物提供碳、氮等養(yǎng)料,但過高質量濃度的CN-反而會抑制微生物的活性,經氧化沉淀處理后,廢水中CN-和重金屬離子的質量濃度已達標或接近達標,其對微生物的抑制作用大大降低;二是廢水經氧化沉淀處理后,部分大分子有機物進一步降解為小分子有機物或直接沉淀去除,從而提高了廢水的可生化性。此外,實驗過程中還考察了BAF對Cu2+和Ni2+的去除效果,發(fā)現(xiàn)BAF置于預處理后及氧化沉淀處理后時,對Cu2+的去除率分別可達40%和80%,而對Ni2+均幾乎沒有去除效果。
3 結論
采用預處理一氧化沉淀-BAF組合工藝處理混合電鍍廢水具有一定的可行性。通過實驗研究,得出以下結論:
(1)確定最佳預處理條件為:初始pH值10,F(xiàn)eS04•7H2O 1 200 mg/L,反應時間15 min。此時,Cr( VI),CN-,Cu2+,Ni2+的去除率分別可達99%,52%,90%,83%,出水中Cr( VI)的質量濃度小于0.5 mg/L。
(2)預處理后,對廢水進行氧化沉淀處理,一方面是為了完全破除氰化物,使廢水達標排放;另一方面是為了破除金屬配位物的配位鍵,使金屬離子游離出來,最后通過沉淀去除。
(3)利用BAF處理氧化沉淀處理后的出水,在水力停留時間為3h時,CODcr的去除率可達50%。同時,BAF對CN-和Cu2+均具有較好的去除效果。
在條件允許時,可將有機物的質量濃度較高的廢水單獨分流出來,并對其進行強化預處理,以使BAF進水中CODcr,的質量濃度小于160 mg/L,確保出水中CODcr的質量濃度達到排放標準。
參考文獻:
[1]茹振修,劉夜月,柴路修,等.堿性條件下處理含氰含鉻混合電鍍廢水[J].給水排水,2000,26(8):36-38.
[2]彭昌盛,孟洪,張維和,等.堿性條件下化學法處理大同齒輪廠混合電鍍廢水[J].環(huán)境工程,2001,19(6):24-25.
[3]郭壯,還原沉淀法處理含鉻廢水的研究及應用[D].哈爾濱:哈爾濱工業(yè)大學,2007.
[4]熊正為,硫酸亞鐵法處理電鍍含氰廢水的試驗研究[J].湖南科技學院學報,2007,28(9):49-52.
[5]陳華進,硫酸亞鐵法處理高濃度含氰廢水[J].工業(yè)水處理,2009,29(10):86-88.
[6]周繼森,易求實,鐵鹽共沉淀法高效簡便去除生活飲用水中的鉻[J].湖北教育學院學報,2001,18(2):44-48.
[7]邢偉,黃文敏,李郭海,等.鐵鹽除磷技術機理及鐵鹽混凝劑的研究進展[J].給水排水,2006,32(2):88-91.
[8]滕華妹,劉鍵.含氰電鍍廢水的氯堿法處理[J].江蘇環(huán)境科技,2001,14(3):14-15.
[9]徐麗花,李亞新,一種好氧生物處理有機廢水的新工藝設備——生物曝氣濾池[J].給水排水,1999,25 (11):1-4.
[10]陳志偉,汪曉軍.曝氣生物濾池對印刷電路板廢水深度處理的研究[J].現(xiàn)代化工,2010,30(5):70-74.
[11] AKCIL A. Destruction of cyanide in goid mill effluents:Biological versus chemical treatments[J]. BiotechnologyAdvances, 2003,21(6):501-511.