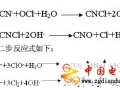
處理電鍍含銀廢水中沉淀劑選擇對比實驗研究
陳明
四川省攀枝花市環(huán)境監(jiān)測站 617000
【摘要】根據(jù)“破除絡(luò)合劑一沉淀”的化學處理工藝處理電鍍含銀廢水為研究背景,通過硫化鈉沉淀法、氫氧化鈉沉淀法、氨水沉淀法在相同的實驗條件下對電鍍含銀廢水進行對比沉淀實驗,通過實驗得知,硫化鈉法來沉淀銀,容易產(chǎn)生刺鼻的硫化氫氣體,氨水淀法沉淀不好控制,如果條件掌握不好就會形成膠體溶液,甚至是己經(jīng)凝聚的膠體沉淀還會因膠溶作用而重新分散到溶液中,此方法對 PH 控制要求非常高,因為如果加入的氨水過量,生成的沉淀與過量的氨水反應(yīng),會發(fā)生銀鏡反應(yīng);氫氧化鈉來沉淀則可以避免上述的問題。
【關(guān)鍵詞】電鍍含銀廢水;沉淀劑;對比試驗
1、前言
隨著現(xiàn)代科技的日新月異,日常生活使用銀及其化合物的范圍也日益增加。銀以及銀的相關(guān)產(chǎn)品廣泛應(yīng)用于電子、電鍍、感光材料、化工工業(yè)和科研領(lǐng)域。與其他工業(yè)相比,雖然產(chǎn)生的廢水量不是很大,但其廢水的性質(zhì)卻決定了它對環(huán)境的污染影響卻非常嚴重。地球資源的有限、人們對環(huán)境生態(tài)的日益關(guān)心和環(huán)保法律的日趨嚴格使全世界都在走工業(yè)廢物回收、再生和循環(huán)利用的可持續(xù)發(fā)展道路[1]。通過實驗旨在對電鍍含銀廢水的合理處理,確定一種簡單、穩(wěn)定,易于操作且處理費用低、效益明顯的處理方法,盡可能回收有用的金屬銀為的目的,為以后研究電鍍含銀廢水的資源化利用以及實現(xiàn)電鍍含銀廢水的綜合治理積累經(jīng)驗。
2、本次實驗的材料和方法
2.1實驗材料
供試樣品來自某大學金防教研室從事電鍍含銀研究所產(chǎn)生實驗后的廢水,包括廢槽液和清洗液。
2.2 實驗方法
2.2.1硫化鈉沉淀法來沉淀銀
化學沉淀法分離元素,是利用各元素化合物的溶度積的不同采用逐步沉淀的方式來達到分離目的的。沉淀分離是一種經(jīng)典的分離方法,它的原理是利用沉淀劑使不需要的干擾組分 ( 或需要的主成分) 形成沉淀,再通過過濾、洗滌以達到分離的目的。不同難溶物的溶度積 Ksp不同,它們沉淀所需的 pH 值也不同[2]。因此,可以通過調(diào)節(jié)溶液 PH 值達到分離金屬離子的目的。可以查得銀硫化物的溶度積常數(shù) KsP 分別為:6.3×10-50 。
量取一定體積的廢液,在攪拌狀態(tài)下緩慢加入一定量的 6.5% 的硫化鈉溶液,反應(yīng)一段時間后,過濾洗滌,分析檢測濾液中銀的濃度,計算銀沉淀率損失率。從分離實驗過程來看,形成的硫化銀沉淀不僅需要較長時間過濾,而且過濾比較困難。經(jīng)多次過濾后的濾液中仍含有細小的沉淀,濾液仍呈淺黑色,對采用分光光度法檢測濾液中的含銀量造成極大的干擾,無法獲得準確的濾液中銀的含量。加入硫化鈉形成的沉淀難以實現(xiàn)重力聚沉而實現(xiàn)自然沉降。但是,硫化物沉淀物顆粒小,易形成膠體; 硫化物沉淀劑本身在水中殘留,遇酸生成硫化氫氣體,此外硫化劑的價格較高。
2.2.2 氫氧化鈉沉淀法來沉淀銀
氫氧化鈉沉淀法處理電鍍含銀廢水原理:此沉淀法是通過投加化學沉淀劑發(fā)生化學反應(yīng),生成難溶的化學物質(zhì),呈沉淀析出。根據(jù)沉淀溶解平衡原理,難溶化合物 AB 的飽和溶液中,存在如下平衡關(guān)系[3]
[A+][B-] = Ksp (2--1)
上式中,Ksp 為難溶化合物的溶度積常數(shù),簡稱溶度積,兩種離子A+、B- 在溶液中可能出現(xiàn)下列三種情況之一:
[A+][B-]
[A+][B-]=Ksp 溶液飽和,但不析出沉淀;
[A+][B-]>Ksp 溶液達飽和,必有難溶化合物從溶液中沉淀析出;顯然,對于難溶性氫氧化物 M(OH)n(n 為金屬 Mn+離子的價態(tài) ) 同樣有:
M(OH)n= nOH-+Mn+
Ksp = [Mn+][OH-]n
式中:Mn+------- 金屬離子濃度
Ksp------- 沉淀溶度積常數(shù)
可見,M(0H)n 沉淀的形成條件是離子積大于其溶度積。根據(jù)公式(2--2) 可知,經(jīng)氫氧化物沉淀法處理金屬離子廢水,其出水濃度能否達到國家排放標準,不僅取決于 Ksp 的大小,而且還與溶液中 0H- 離子的濃度有關(guān)。結(jié)合公式 (2--2) 以及水的離子積 Kw=[H-][OH+] 可得氫氧化物沉淀形式的 PH 值:
pH = 14 - l/n(lg[Mn+] 一 lgksp) (2--3)