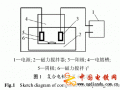
―、氯化梓
1.方法摘要
在pH為10的溶液中,鋅與EDTA生成穩(wěn)定的絡(luò)合物,以鉻黑T為指示劑,反應(yīng)式如下:

2.試劑
(1)緩沖溶液(pH為10):溶解54g氯化銨于水中,加入350mL氨水(比密度0.89), 加水稀釋至1L。
(2)鉻黑丁指示劑。
(3)標(biāo)準(zhǔn)0.05 mol EDTA 溶液:稱取 EDTA 20g,以水加熱溶解后,冷卻,稀釋至1L。
標(biāo)定:稱取分析純金屬鋅0.4g(四位有效數(shù)字)于100mL小燒杯中,以少量1:1鹽酸溶解(加蓋小表面皿于小燒杯上),加熱使溶解完全,冷卻,移入100mL容量瓶中,加水稀釋至刻度,搖勻。用移液管吸取20mL于250mL錐形瓶中,加水50mL,以氨水調(diào)節(jié)至微氨性,加入pH為10的緩沖溶液10mL及鉻黑T指示劑數(shù)滴,搖勻,以配制好的約0.05 mol EDTA標(biāo)準(zhǔn)溶液滴定至紅色變藍(lán)色為終點(diǎn)。

式中,M為標(biāo)準(zhǔn) EDTA 溶液的摩爾濃度;V為耗用標(biāo)準(zhǔn) EDTA 溶液的毫升數(shù);P為鋅質(zhì)量(g)。
3.分析方法
用移液管吸取鍍液2mL于250mL錐形瓶中,加水50 mL ,加緩沖溶液10 mL ,鉻黑T 數(shù)滴,立刻以 EDTA 滴定至溶液由酒紅色變?yōu)樗{(lán)色為終點(diǎn)。
4.計(jì)算

式中,M為標(biāo)準(zhǔn) EDTA 溶液的摩爾濃度;V為耗用標(biāo)準(zhǔn) EDTA 溶液的毫升數(shù)。
5.附注
(1)本方法只適用于雜質(zhì)不太多的鍍液;
(2)取樣加水后,夏天可用冷浴冷卻(各個(gè)試液的冷卻時(shí)間要一樣長)使終點(diǎn)較為 美觀;
(3)滴定速度以稍快一些為好;
(4)也可加焦磷酸鈉或氟化鉀以掩蔽鐵后,用 EDTA 滴定。或加1%銅試劑3mL作為 銅的掩蔽劑。
二、氯化鉀
1.方法摘要
以標(biāo)準(zhǔn)硝酸銀與氯化鉀生成氯化銀沉淀,過量的銀與鉻酸鉀生成磚紅色的鉻酸銀為終點(diǎn)。

2.試劑
(1)1%鉻酸鉀溶液。
(2)標(biāo)準(zhǔn)0.1 mol 硝酸銀溶液。
配制:取分析純硝酸銀于120°C干燥2h,在干燥器內(nèi)冷卻,準(zhǔn)確稱取17.000g,溶解于水,在容量瓶中稀釋至1000mL。儲于棕色瓶中,不需標(biāo)定。
3.分析方法
用移液管吸取鍍液1 mL 于250 mL 錐形瓶中,加水50 mL 、1%鉻酸鉀2?5滴,以 0.1 mol 硝酸銀溶液滴定至由黃色變?yōu)榇u紅色為終點(diǎn)。
4.計(jì)算
![]()